公益培训 | 河南省第五期“UDI合规与实操培训班”!
2021-03-17

**峰会背景**
2020年9月30日,国家药品监督管理局发布了唯一标识系统试点时间延长至2020年12月31日,从原来的9大类64个品种的基础上又增加了5种高风险产品纳入了第一批实施产品目录中。第一批实施唯一标识的医疗器械注册人将于2021年1月1日起,严格按照《医疗器械唯一标识系统规则》等相关要求开展产品赋码、数据上传和维护等工作。
为帮助企业解决UDI实施过程中的问题,**中广汇智·UDI公共平台联合中国食品药品企业质量安全促进会医疗器械分会与河南省医疗器械商会**定于2021年3月19日在河南郑州举办第五期“医疗器械唯一标识(UDI) 合规与实操培训班”, 培训班将围绕UDI设计, 从宏观政策到具体标准,从基本概念到应用实施, 针对UDI编码、UDI标签设计、上报数据库、UDI扩展应用、产品溯源防伪等进行。
**组织机构**
**主办单位:**
中广汇智·UDI公共平台
中国食品药品企业质量安全促进会医疗器械分会
河南省医疗器械商会
**学术支持:**
中关村工信二维码技术研究院
湖南中广汇智信息技术有限公司
**培训内容**
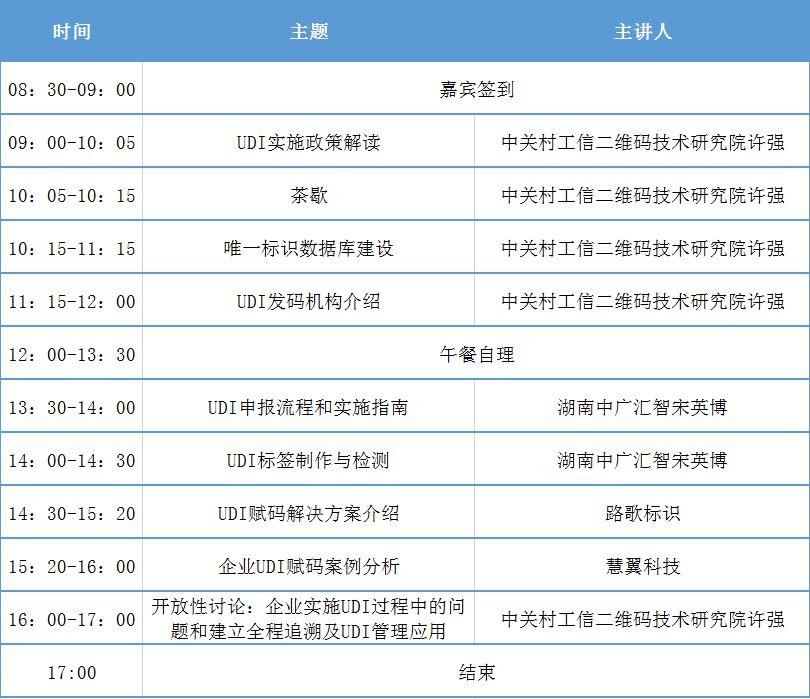
**培训对象**
1、从事医疗器械注册、研发、管理、质量法规、临床、及生产相关人员
2、科研单位从事医疗器械研发与管理的相关人员
3、创新创业团队或个人
**培训意义**
1、掌握医疗器械UDI相关法律法规知识
2、简化申报流程,节约申报时间成本和人工成本,提高申报效率
3、提升企业信息化水平,提高企业生产效率
**时间地点**
**时间:**2021年3月19日
**地点:**河南郑州(具体酒店信息关注邮箱或短信)
**温馨提示**
**本次培训属于公益培训,培训免费,食宿自理。**
**报名入口(长按识别,填写表单)**

为帮助各大企业答疑解难,尽快完成UDI实施,**UDI公共平台近期还将举办一系列讲座**。

★重磅!《医疗器械监督管理条例(修订草案)》正式通过!
★三级医院、医械公司,一次性被重罚超200万元!这个315,你该了解一下医疗器械UDI!
★2021(第二届)大湾区医疗器械唯一标识(UDI)峰会暨医疗器械唯一标识(UDI)合规实操公益培训成功召开!
★政策解读|福建省《关于全面推进医疗器械唯一标识系统建设工作的通知》
★河北省药监局召开会议:加快推进医疗器械唯一标识(UDI)工作!

上一篇:【UDI公共平台er每日早报】
下一篇:【UDI公共平台er每日早报】
UDI资料免费获取
UDI实施报告及UDI政策汇编
 免费获取
免费获取
×


